Le glaucome à pression normale est une entité clinique particulière susceptible
de poser des problèmes sur le plan du diagnostic, des facteurs de risque comme de la prise en charge.
Introduction
Le glaucome est une neuropathie optique chronique progressive, marquée par des modifications anatomiques de la tête du nerf optique (TNO) associées à des altérations du champ visuel (1). La notion d’hypertonie oculaire (HTO) n’est plus mise en avant comme cela pouvait être le cas dans le passé : l’absence d’HTO n’élimine pas le diagnostic de glaucome et, si l’on prend ce critère en considération, on est susceptible de ne pas diagnostiquer un glaucome sur deux (2). Von Graefe a été le premier à identifier une excavation papillaire survenant sans HTO associée (3), cette notion a été reprise plus tardivement (4). Le glaucome à pression normale (GPN) est à présent décrit comme un glaucome primitif à angle ouvert sans HTO associée, et on considère que GPN et GPAO font partie de la même entité clinique (5).
Épidémiologie
Les données épidémiologiques concernant le GPN sont peu nombreuses, relativement variables et non univoques en termes d’interprétation. La proportion de GPN varie de 6 % à plus de 70 % (6, 7) des glaucomes à angle ouvert. La prévalence du GPN est beaucoup plus importante en Asie, et notamment au Japon (6) (Fig. 1).
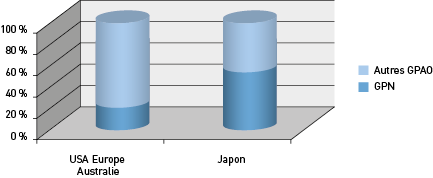
Figure 1 – Proportion des GPN et autres GPAO qui diffère en fonction de l’origine géographique.
La lecture de cet article est réservée aux abonnés.
Pour accéder à l'article complet
Découvrez nos offres d'abonnement
Abonnez-vous à la revue et accédez à tous les contenus du site !
- Tous les contenus de la revue en illimité
- Les numéros papier sur l'année
- Les newsletters mensuelles
- Les archives numériques en ligne
ou
Article épuisé !
Non disponible à la vente.
ou
Inscrivez-vous gratuitement sur Mon Œil.fr et bénéficiez de l'accès à de nombreuses catégories du site !
- Accès aux catégories d'articles exclusives
- Les newsletters mensuelles
- Votre historique de commandes en ligne